ulasan asam
Pernah bertanya-tanya mengapa Anda bisa meminum asam yang ditemukan dalam jus jeruk, tetapi tidak dapat meminum asam di aki mobil Anda?
Kedua asam ini memiliki konsentrasi yang berbeda. Ternyata struktur molekul senyawa tersebut dapat mempengaruhi kekuatan asam. Mari cari tahu lebih lanjut tentang bagaimana struktur memengaruhi kekuatan asam.
Untuk menentukan seberapa asam suatu zat, seorang ahli kimia dapat mengukur pH , yang didasarkan pada jumlah asam dalam larutan. Semakin rendah pH, semakin asam larutan tersebut.
Jika Anda memiliki sedikit asam kuat, seperti asam sulfat, dalam larutan, mungkin memiliki pH yang lebih tinggi (kurang asam) daripada jika Anda memiliki banyak asam lemah seperti asam sitrat dalam larutan. Jumlah asam itu penting.
Ahli kimia juga dapat menggunakan pKa untuk menilai keasaman, yang tidak didasarkan pada jumlah asam. Nilai pKa menggambarkan berapa banyak ion asam yang akan dihasilkan suatu zat dalam suatu larutan.
Misalnya, Anda memiliki dua larutan dengan jumlah molekul asam sulfat yang sama di salah satunya dan asam sitrat di larutan lainnya. Larutan asam sulfat akan lebih asam karena asam sulfat kehilangan lebih banyak proton untuk menghasilkan lebih banyak ion hidronium (H 3 O + ).
Mirip dengan pH, semakin rendah pKa, semakin kuat asamnya. Jadi asam sulfat memiliki pKa lebih rendah dari asam sitrat (-3 vs 3.1).
Ada jutaan bahan kimia di dunia dan akan sangat sulit untuk mengukur semua nilai pKa untuk masing-masingnya. Oleh karena itu, kami melihat kesamaan dalam struktur untuk membantu kami memprediksi nilai-nilai ini.
Resonansi
Asam ada dalam kesetimbangan dengan basa konjugatnya. Kekuatan asam (pKa) tergantung pada kestabilan basa. Ketika proton meninggalkan asam, ia meninggalkan elektronnya. Mereka supernegatif dan ada muatan negatif yang besar pada basis konjugatnya.
Anda tahu bahwa jika ada muatan negatif yang terkonsentrasi, basa tidak terlalu stabil. Namun, jika muatannya dapat menyebar, maka basa lebih stabil, yang berarti kita memiliki asam yang lebih kuat. Jika sebuah molekul memiliki elektron yang tersebar di lebih dari satu ikatan, ia memiliki resonansi .
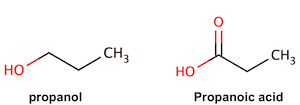
Jadi menurut Anda mana yang memiliki pKa lebih rendah: propanol atau asam propanoat?
|
|
|
Molekul manakah yang memiliki pKa lebih rendah? |
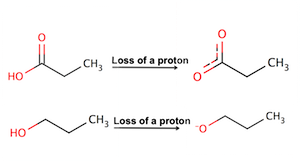
Jika Anda memilih asam propanoat, Anda benar! Ketika asam propanoat kehilangan proton, dua molekul oksigen berbagi muatan negatif, memberikannya resonansi dan dengan demikian menstabilkan basa dan menghasilkan asam kuat. Ketika propanol kehilangan proton, tidak ada resonansi.
|
|
|
Ketika proton dihilangkan dari asam propanoat, muatan negatif dibagi antara dua atom oksigen, menjadikannya asam yang lebih kuat daripada propanol. |
ukuran atom
Ingat, asam yang lebih kuat memiliki basa yang lebih stabil. Salah satu hal yang mempengaruhi stabilitas basa adalah ukuran ion. Ion yang lebih besar dapat menampung muatan negatif dengan lebih baik. Bayangkan beban memiliki lebih banyak “ruang” untuk menyebar.
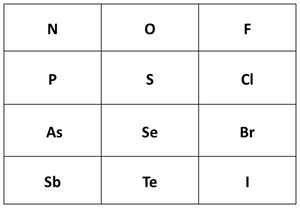
Untungnya, kita dapat menggunakan tren periodik untuk memprediksi ukuran ion. Ini berarti bahwa kita dapat memprediksi basa paling stabil dan asam terkuat. Ukuran ion bertambah dari atas ke bawah dalam kolom tabel periodik. (Ukuran ion juga bertambah dari kanan ke kiri, tetapi itu tidak mempengaruhi stabilitas basa karena keelektronegatifan, yang akan kita bicarakan sebentar lagi.)
|
|
|
Ukuran atom meningkat saat Anda turun kolom dalam tabel periodik. |
Jadi manakah yang memiliki pka lebih rendah, asam klorida (HCl) atau asam hidrobromat (HBr)?
Jika Anda menjawab asam hidrobromat, Anda benar! Br – lebih besar dari Cl – . Ini berarti bahwa Br – merupakan basa yang lebih stabil, sehingga HBr merupakan asam yang lebih kuat. pKa HBr adalah -9, sedangkan pKa HCl adalah -7.
keelektronegatifan
Ingatlah bahwa keelektronegatifan adalah kemampuan atom untuk menarik elektron. Keelektronegatifan meningkat dari kiri ke kanan dalam deretan tabel periodik. Ini juga meningkat saat Anda naik kolom, tetapi ukuran atom lebih memengaruhi keasaman. Bayangkan itu sebagai pertarungan. Keelektronegatifan ‘menang’ secara horizontal pada tabel periodik, sedangkan ukuran atom ‘menang’ secara vertikal.
Jika sebuah atom sangat elektronegatif, ia dapat menampung elektron ekstra yang tertinggal ketika asam kehilangan sebuah proton. Oleh karena itu, pangkalan lebih stabil.
|
|
|
Keasaman molekul meningkat dengan meningkatnya keelektronegatifan saat Anda bergerak dari kiri ke kanan pada tabel periodik. Ketika ukuran kolom meningkat, begitu pula keasamannya. |
Jadi mana asam HCl atau H2S yang lebih kuat?
Jika Anda memilih HCl, Anda benar! Cl lebih elektronegatif daripada S, jadi “lebih bahagia” ketika memiliki elektron ekstra dibandingkan dengan S. Jadi Cl – adalah basa yang lebih stabil dan HCl adalah asam yang lebih kuat.
efek induktif
Tahukah Anda bahwa ketika atom elektronegatif berikatan di dekat asam hidrogen, hal itu dapat memengaruhi pKa? Atom elektronegatif akan menarik kerapatan elektron, yang akan membantu menstabilkan muatan negatif yang tertinggal saat proton dihilangkan. Artinya basa akan lebih stabil dan akan menghasilkan asam yang lebih kuat.
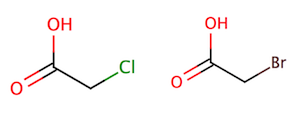
Manakah asam yang lebih kuat: asam bromoasetat atau asam kloroasetat?
|
|
|
Apakah asam kloroasetat atau asam bromoasetat adalah asam yang lebih kuat? |
Jika Anda memilih asam kloroasetat, Anda benar! Klor lebih elektronegatif daripada brom, sehingga menarik lebih banyak kerapatan elektron, menstabilkan basa konjugasi asam.
Semakin dekat atom elektronegatif dengan hidrogen asam, semakin banyak ia menarik kerapatan elektron, menghasilkan asam yang lebih kuat.
Ringkasan Pelajaran
Struktur molekul dapat digunakan untuk memprediksi keasaman suatu senyawa. PH suatu larutan tergantung pada konsentrasi asam. PKa menjelaskan berapa banyak ion asam yang akan dihasilkan suatu zat dalam larutan atau, dalam kasus kita, ini menunjukkan berapa banyak proton yang terdisosiasi membentuk ion hidronium. Semakin rendah pKa, semakin kuat asamnya. Beberapa elemen struktural molekul dapat mempengaruhi pKa, termasuk:
- Resonansi – Jika sebuah molekul memiliki elektron yang menjangkau lebih dari satu ikatan (jika sebuah molekul memiliki resonansi), ia akan memiliki pKa yang lebih rendah dibandingkan dengan molekul yang tidak.
- Ukuran Atom : Ketika ukuran atom meningkat dalam kolom tabel periodik, keasaman meningkat.
- Keelektronegatifan – Kemampuan suatu atom untuk menarik elektron. Ketika elektronegativitas atom meningkat dari kiri ke kanan berturut-turut, keasaman meningkat.
- Efek Induktif : Atom elektronegatif akan menarik kerapatan elektron, menstabilkan basa konjugat. Ini meningkatkan keasaman molekul.