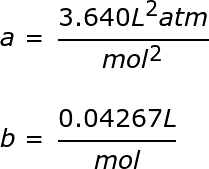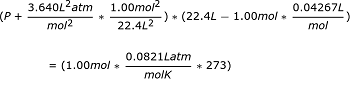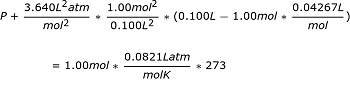Gas nyata berperilaku berbeda
Dalam pelajaran lain, kita mempelajari bagaimana perilaku gas nyata menyimpang dari perilaku gas ideal dalam kondisi tidak ideal. Mereka berperilaku berbeda karena kondisi tidak ideal ini cukup menegangkan: tekanan dan kepadatan yang sangat tinggi, dan suhu yang sangat rendah. Untuk memperhitungkan perubahan ini, kita perlu sedikit memodifikasi hukum gas ideal. Perubahan ini termasuk konstanta yang mengukur volume molekul gas, serta gaya tarik menarik antara molekul tersebut, yang dianggap dapat diabaikan dalam kondisi ideal.
Awalnya, hukum gas ideal terlihat seperti ini: PV = nRT . P adalah tekanan dalam atmosfer, V adalah volume wadah dalam liter, n adalah jumlah mol gas, R adalah tetapan gas ideal (0,0821 L-atm/mol-K), dan T adalah temperatur dalam Kelvin .
Untuk gas nyata, kami membuat dua perubahan dengan menambahkan konstanta ke suku tekanan ( P ) dan mengurangkan konstanta yang berbeda dari suku volume ( V ). Persamaan baru terlihat seperti ini: ( P + an 2 ) ( V – nb ) = nRT . Di sini, a adalah konstanta tarik-menarik antara molekul-molekul gas tertentu (pikirkan a untuk tarik -menarik ), dan b adalah volume yang diambil molekul-molekul tersebut di dalam wadah.
Anda mungkin telah memperhatikan beberapa n yang aneh diberi label bersama dengan kedua konstanta tersebut, dan itu karena a dan b adalah nilai untuk satu mol gas itu. Jadi kita harus mengalikan konstanta dengan jumlah total mol untuk mendapatkan nilai yang benar. Dan ingat, konstanta berbeda untuk setiap gas karena setiap gas memiliki sifat yang berbeda.
Menggunakan persamaan Van Der Waals
Persamaan baru ini disebut persamaan van der Waals , diambil dari nama ilmuwan Belanda Johannes van der Waals, yang melakukan banyak pekerjaan untuk menemukan bagaimana perilaku gas nyata. Meskipun persamaan ini terlihat berbeda dari hukum gas ideal, Anda masih bisa menyelesaikannya dengan cara yang sama selama Anda mengetahui variabel lainnya. Perbedaannya di sini adalah Anda juga perlu mengetahui nilai konstanta a dan b , yang untungnya bagi kami, tersedia dan dapat dicari dengan mudah.
Untuk melihat bagaimana perilaku gas nyata, mari kita mulai dengan contoh sederhana menggunakan hukum gas ideal. Katakanlah kita memiliki gas CO 2. Kami memiliki 1,00 mol ( n ), pada 273 K ( T ), dan berada dalam wadah dengan volume 22,4 L ( V ). Untuk memecahkan tekanan ( P ), kita cukup mengatur ulang persamaan dan menghitungnya.
Apa yang kami temukan adalah bahwa:
|
|
Sekarang mari kita cari tekanan menggunakan persamaan van der Waals. Ingat, semuanya sama, kecuali sekarang kita perlu memasukkan a dan b . Untuk CO2,
|
|
Begini tampilannya sekarang:
|
|
Apa yang sekarang kita temukan adalah bahwa P = 0,995 atm. Itu cukup dekat dengan jawaban pertama kami, jadi apa yang terjadi di sini? Nah, pada suhu dan tekanan normal, pada dasarnya kita akan mendapatkan hasil yang sama dengan menggunakan hukum gas ideal atau persamaan van der Waals. Jadi yang harus kita lakukan adalah menguji gas ini dalam kondisi yang cukup ekstrem.
Mari kita coba lagi, tetapi kali ini, mari kita ubah volume wadah menjadi jauh lebih kecil, katakanlah 0,100 L. Kita memperkirakan tekanan akan meningkat karena ruang untuk menyerap gas semakin sedikit, yang berarti molekul-molekul akan bertabrakan di dinding wadah wadah lebih sering.
Menggunakan hukum gas ideal, kami menemukan itu
|
|
Itu banyak tekanan!
Sekarang mari kita lihat bagaimana ini menyimpang ketika kita menggunakan persamaan van der Waals untuk perilaku gas yang sebenarnya. Jika kita memasukkan variabel kita, kita mendapatkan:
|
|
Tekanan kita sekarang hanya 31,5 atm. Lihat bagaimana P sangat berbeda dibandingkan jika kita menggunakan hukum gas ideal?
Ini masih merupakan tekanan yang lebih tinggi dari kondisi ideal, tetapi mengapa jauh lebih rendah dari hasil yang kami peroleh dari persamaan gas ideal? Hal ini karena dengan menggunakan persamaan van der Waals, kita memperhitungkan gaya tarik menarik yang kuat antara molekul CO 2. Saat molekul didorong ke ruang yang lebih sempit, mereka memang lebih sering bertabrakan dengan dinding wadah, tetapi mereka juga tetap berdekatan karena gaya tarik meningkat saat mereka tergencet ke ruang yang lebih sempit.
Ringkasan Pelajaran
Dengan menggunakan hukum gas ideal, kita dapat menemukan tekanan, volume, suhu, atau jumlah mol gas ideal. Tapi untuk gas nyata, kita perlu menggunakan persamaan van der Waals karena memperhitungkan efek volume relatif dari molekul gas, serta daya tarik antar molekul tersebut. Namun, begitu kita memasukkan konstanta ini ke dalam persamaan, proses penyelesaian variabel yang hilang adalah sama.
Persamaan van der Waals ditulis seperti ini: ( P + an 2 / V 2 ) ( V – nb ) = nRT . Ini sangat mirip dengan hukum gas ideal ( PV = nRT ), kecuali sekarang kami menjelaskan gaya tarik antara molekul gas dengan a , dan volume molekul tersebut dengan b . n juga digunakan beberapa kali lagi karena volume dan daya tarik adalah nilai hanya untuk satu mol gas tertentu itu. Jadi kita cukup mengalikan setiap konstanta yang kita cari dengan jumlah total mol gas untuk mendapatkan jumlah yang tepat.
hasil pembelajaran
Dengan menyelesaikan pelajaran video ini, Anda dapat bersiap untuk menggunakan persamaan van der Waals untuk menyelesaikan perilaku gas aktual versus persamaan gas ideal.