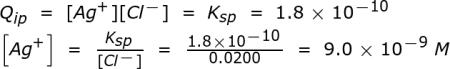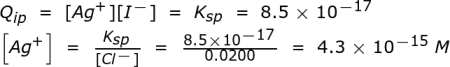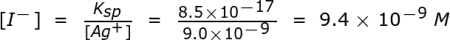Memisahkan Adalah Rasa Sakit Yang Manis: Memisahkan Ion Secara Selektif
Pernahkah Anda memiliki keinginan untuk memisahkan cokelat Anda dari selai kacang teman Anda atau selai kacang teman Anda dari cokelat Anda? Yah, itu mungkin bukan situasi yang sangat kritis, tetapi dalam analisis kimia, kita sering perlu menghilangkan ion secara selektif dari suatu larutan agar dapat menganalisis yang lain atau menghilangkan ion yang mungkin mengganggu analisis larutan lebih lanjut. Di sinilah kami memperkenalkan presipitasi selektif , yang merupakan kemampuan untuk menghilangkan semua atau sebagian besar ion dari larutan tanpa mempengaruhi konsentrasi spesies lain secara signifikan.
Misalnya, katakanlah Anda memiliki larutan yang mengandung ion klorida dan sulfat dan Anda perlu menghilangkan ion sulfat karena akan mengganggu reaksi klorida lebih lanjut. Anda dapat mengendapkan sulfat dengan menambahkan larutan barium hidroksida. Hasilnya adalah endapan barium sulfat yang tidak larut dalam air sedangkan barium klorida yang terbentuk tetap berada dalam larutan. Jika Anda pernah menjalani rontgen GI, Anda mungkin sangat akrab dengan barium sulfat, karena ini adalah agen kontras utama yang ditemukan dalam cairan asam yang kurang menyenangkan yang Anda minum sebelum rangkaian rontgen Anda siap. .
Anda mungkin ingat bahwa banyak senyawa ionik yang tidak sepenuhnya larut atau tidak larut dalam larutan, tetapi tetapkan kesetimbangan pada titik jenuh antara zat terlarut padat dan keadaan terlarutnya. Kesetimbangan dalam saturasi zat terlarut ini memiliki konstanta kesetimbangan terkait, K sp , dan disebut produk kelarutan . Produk kelarutan dan produk ionik , Q ip (nilai zat terlarut dan konsentrasi ion di luar kesetimbangan), dapat digunakan untuk memprediksi apakah pengendapan akan terjadi dan konsentrasi apa yang diperlukan untuk melakukannya.
Hal ini memungkinkan kita untuk menentukan apakah ion tertentu dapat diendapkan (dipisahkan) secara selektif dari larutan tanpa mempengaruhi ion lain. Dalam kesetimbangan, Q ip = K sp . Jika Q ip lebih besar dari K sp , akan terjadi pengendapan dan jika Q ip lebih kecil dari K sp , tidak akan terjadi pengendapan.
selektif
Mari kita lihat situasi di mana kita memiliki larutan ion halida, klorida, dan iodida, yang ingin kita pisahkan secara efektif untuk kemudian mengisolasi ion klorida. Konsentrasi setiap ion dalam larutan masing-masing adalah 0,0200 M. Kami memiliki larutan perak nitrat 2,00 M, AgNO 3 . Bisakah kita menggunakan ini untuk memisahkan ion halida ini secara selektif? Pertama, mari kita lihat nilai K sp untuk endapan yang diharapkan dari perak klorida dan perak iodida.
|
Menggabungkan |
Ksp |
|
AgCl |
1,8 x 10 -10 |
|
AgI |
8,5×10-17 |
Kami melihat dari tabel ini bahwa ada hampir tujuh kali lipat perbedaan antara produk kelarutan masing-masing untuk senyawa ini, jadi sangat mungkin kami dapat memisahkannya. Saat ini terjadi, kita dihadapkan pada pertanyaan yang mungkin Anda pikirkan saat mencoba memisahkan selai kacang dari cokelat: apa yang akan terjadi lebih dulu? Atau dalam kasus percobaan kita di sini, ion manakah yang akan mengendap terlebih dahulu?
Pertama datang, pertama dilayani (atau bergegas)
Kami memiliki konsentrasi dan nilai K sp yang diketahui untuk dua halida kami dan kami ingin tahu mana yang akan mulai mengendap terlebih dahulu. Yang perlu kita ketahui adalah berapa konsentrasi perak, [Ag + ], yang diperlukan untuk memulai proses pengendapan setiap ion. Ini akan menjadi titik di mana Q ip = K sp . Pertama mari kita mulai dengan menghitung titik ini untuk ion klorida:
|
|
Mari kita ulangi perhitungan serupa untuk ion iodida:
|
|
Artinya, ketika konsentrasi Ag+ mencapai 4,3 x 10 -15 M, iodida akan mulai mengendap sebagai AgI, tetapi klorida tidak akan karena konsentrasi Ag+ harus mencapai 9,0 x 10 -9 M sebelum itu. mulai mengendap sebagai AgCl.
Tetap dibelakang
Sekarang kita tahu berapa konsentrasi Ag + masing-masing akan mulai mengendap, kita perlu mengetahui berapa banyak iodida yang tersisa dalam larutan ketika klorida mulai mengendap. Untuk menentukan [I – ] yang tersisa tepat ketika klorida mulai mengendap, kita perlu mengatur ulang ekspresi K sp untuk menyelesaikan [I – ] menjadi [Ag + ] yang diketahui.
|
|
Membandingkan konsentrasi iodida akhir 9,4 x 10 -9 M dengan konsentrasi awal 0,0200 M, terlihat perbedaan yang besar. Untuk melihatnya dengan lebih mudah, mari kita lihat persen konsentrasi yang tersisa untuk ion iodida.
|
|
Karena standar tipikal yang digunakan untuk kelengkapan pengendapan ditetapkan sebesar 0,1% tersisa dan kita jauh di bawah tanda tersebut, kita dapat dengan aman mengatakan bahwa kita dapat secara selektif mengendapkan dan memisahkan kedua ion halida ini dari larutan dan dari satu sama lain.
Ringkasan Pelajaran
Mari kita tinjau apa yang telah kita pelajari dalam pelajaran ini. Ada banyak kasus dalam analisis kimia yang sangat berguna untuk memisahkan ion untuk membantu analisis. Hal ini dapat dilakukan dengan presipitasi selektif, yaitu kemampuan untuk menghilangkan semua atau sebagian besar ion dari larutan tanpa mempengaruhi konsentrasi spesies lain secara signifikan.
Kami juga belajar bahwa untuk menghitung apakah pemisahan seperti itu mungkin, perlu dipahami bagaimana produk kelarutan (konsentrasi spesies pada kesetimbangan dan saturasi) dan produk ionik (nilai konsentrasi zat terlarut dan ion di luar kesetimbangan) mempengaruhi kesetimbangan kelarutan. . Selain itu, perbedaan hasil kali kelarutan dapat berfungsi sebagai indikator tentatif jika pemisahan dapat terjadi bahkan sebelum menghitung kondisi pengendapan yang diperlukan. Semakin besar perbedaan produk kelarutan, semakin besar kemungkinan pemisahan.