Pengertian Ikatan Ion dan Transfer elektron – Ikatan ion adalah hasil dari transfer elektron dari unsur logam ke unsur non-logam.
Ikatan Ion
Ikatan ion adalah jenis ikatan kimia di mana elektron valensi hilang dari satu atom dan diperoleh dari atom yang lain. Hasil pertukaran ini secara lebih stabil, konfigurasi elektron gas mulia untuk kedua atom yang terlibat. Ikatan ion didasarkan pada gaya tarik elektrostatik antara dua muatan ion yang berlawanan.
Kation dan Anion
Ikatan ion melibatkan kation dan anion. Ikatan tersebut terbentuk ketika sebuah atom, biasanya logam, kehilangan satu elektron atau lebih banyak elektron, dan menjadi ion positif, atau kation. Atom lain, biasanya non-logam, mampu memperoleh satu atau lebih elektron dan menjadi ion negatif, atau anion.
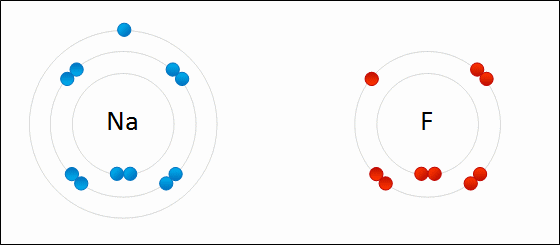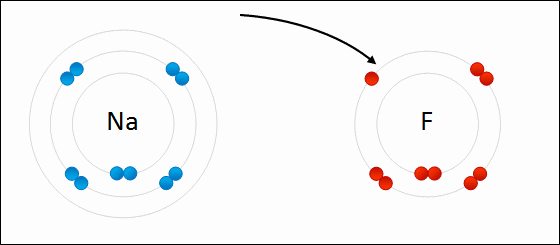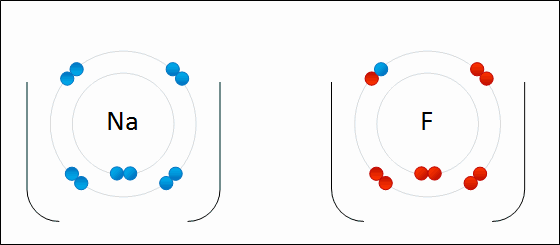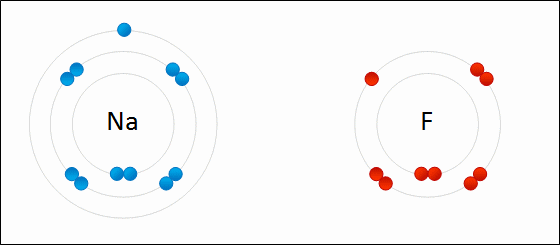
Salah satu contoh dari ikatan ion adalah pembentukan natrium fluoride. NaF, dari atom natrium dan atom fluorin. Dalam reaksi ini, atom natrium kehilangan satu elektron valensi ke atom fluorin, yang memiliki cukup ruang untuk menerimanya. Ion-ion yang dihasilkan malah bermuatan dan tertarik satu sama lain karena gaya elektrostatik.
Pada skala makroskopik, senyawa ion membentuk kisi, kisi adalah padatan kristal dalam kondisi normal, dan memiliki titik leleh yang tinggi. Sebagian besar ini adalah zat larut dalam H2O dan menghantarkan listrik bila dilarutkan. Kemampuan untuk menghantarkan listrik dalam larutan oleh karena itu zat ini disebut elektrolit. Garam meja, NaCl, adalah contoh dari jenis senyawa ini.
Ikatan ion berbeda dari ikatan kovalen. Kedua jenis mengakibatkan keadaan elektron yang stabil terkait seperti gas mulia. Namun, dalam ikatan kovalen, elektron dibagi antara dua atom. Semua ikatan ion memiliki beberapa karakter kovalen, namun semakin besar perbedaan elektronegativitas antara dua atom, semakin besar karakter interaksi ionik.
Ringkasan
Ikatan ion terbentuk antara kation dan anion.
Sebuah kation terbentuk ketika ion logam kehilangan elektron valensi sedangkan anion terbentuk ketika mendapatkan elektron valensi non-logam. Mereka berdua mencapai konfigurasi elektron yang lebih stabil melalui pertukaran ini.
Ikatan ionik pada zat padat membentuk kisi kristal, atau pengulangan pola atom, dengan titik leleh tinggi, dan biasanya larut dalam air.
Elektronegativitas adalah Kecenderungan atom untuk menarik elektron untuk dirinya sendiri.
Elektrolit adalah Senyawa ionik yang larut dalam H2O, membuat larutan yang dihasilkan mampu menghantarkan listrik.
Kation adalah Ion bermuatan positif.
Anion adalah Ion bermuatan negatif.
