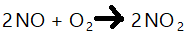Apa itu entalpi?
Bayangkan Anda memiliki dua mobil dan keduanya membutuhkan 30 galon bensin untuk dijalankan, namun yang satu dapat menempuh jarak 100 mil di tangki itu, sementara yang lain menempuh jarak 600 mil. Anda mungkin akan memilih untuk menggunakan tangki 600 mil untuk perjalanan jauh, bukan? Meskipun kedua mobil membutuhkan banyak tenaga, seseorang memanfaatkan tenaga itu dengan lebih baik untuk beroperasi.
Gagasan inilah yang mendorong beberapa reaksi. Seringkali membutuhkan banyak energi untuk mendapatkan reaksi untuk memulainya. Tetapi untuk reaksi yang menguntungkan, tingkat energi akhir biasanya lebih rendah daripada energi awal. Besarnya energi dalam suatu reaksi atau dalam suatu senyawa disebut entalpi .
perubahan entalpi
Entalpi sering digambarkan sebagai jumlah panas dalam suatu sistem. Ketika datang untuk mengukur energi yang terkait dengan entalpi, panas dan energi dapat digunakan secara sinonim. Entalpi sering diukur dengan membakar senyawa dan melihat berapa banyak panas yang dihasilkannya. Sebenarnya yang terjadi saat senyawa dibakar adalah reaksi yang memecah senyawa tersebut. Jadi, perubahan energi (dari senyawa asli ke senyawa yang terdekomposisi) diukur untuk menentukan berapa banyak energi yang mampu dipancarkan oleh senyawa tersebut.
Salah satu cara untuk menggerakkan reaksi adalah dengan memiliki lebih sedikit energi dalam produk daripada dalam reaktan. Ini berarti bahwa perubahan entalpi negatif. Reaksi masih dapat terjadi jika perubahan entalpinya positif, hanya perlu ada hal lain yang mendorong reaksi tersebut. Perubahan entalpi adalah perbedaan entalpi (energi) dari awal reaksi sampai akhir reaksi.
Hitunglah perubahan entalpinya
Untuk menghitung perubahan entalpi, Anda harus terlebih dahulu mengetahui entalpi awal dan akhir. Salah satu cara paling umum untuk melakukannya adalah dengan membakar senyawa (seperti yang disebutkan di atas). Ini dilakukan dalam kalorimeter , yang hanya berupa wadah yang membakar senyawa dan mengukur jumlah panas yang dilepaskan. Tabel yang disebut tabel panas pembentukan akan mencantumkan senyawa umum dan entalpi yang telah dihitung.
Setelah Anda mengetahui entalpi masing-masing bahan awal dan akhir, Anda dapat menentukan perubahan entalpinya. Menggunakan persamaan kimia seimbang, kalikan entalpi setiap senyawa dengan jumlah molekul yang digunakan dalam persamaan setara. Kemudian, cari selisih antara entalpi total semua senyawa pada sisi reaktan dan entalpi total semua senyawa pada sisi produk.
Contoh Perhitungan
Sekarang mari kita lihat sebuah contoh. Mari kita membuat nitrogen dioksida. Nitrogen dioksida diproduksi saat mengendarai mobil Anda dan dalam ledakan vulkanik. Persamaan seimbang untuk memproduksi nitrogen dioksida adalah:
|
|
Jadi dua mol oksida nitrat ditambah satu mol oksigen menghasilkan 2 mol nitrogen dioksida. Kalor pembakaran nitrit oksida 90,4 kJ/mol, kalor pembakaran oksigen 0 kJ/mol, dan kalor pembentukan nitrogen dioksida 33,9 kJ/mol. Kami akan mengacu pada perubahan entalpi (delta H) hanya H dalam persamaan ini.
H = (2 mol * 33,9 kJ/mol) – (2 mol) * 90,4 kJ/mol + 1 mol * 0 kJ/mol)
H = 67.8kJ – 180.8kJ
H = -113kJ
Karena perubahan entalpi negatif, kita dapat melihat bahwa reaksi ini berlangsung berdasarkan energi yang lebih kecil pada produk daripada reaktan.
Ringkasan Pelajaran
Entalpi adalah ukuran energi dalam suatu senyawa atau reaksi. Itu dapat diukur dengan kalorimeter . Entalpi juga dapat ditemukan dalam tabel seperti tabel kalor pembentukan . Perubahan entalpi adalah perbedaan entalpi reaktan vs produk. Perubahan entalpi dapat dihitung dengan mengurangkan entalpi total reaktan dari entalpi total produk. Entalpi setiap senyawa harus dikalikan dengan jumlah mol yang ada dalam persamaan kimia yang seimbang.