Apa itu isomer?
Bayangkan Anda memiliki balok berwarna dengan angka. Anda menyadari bahwa adalah mungkin untuk mengatur ulang blok-blok ini dengan berbagai cara. Anda memutuskan bahwa reorganisasi struktural ini akan melibatkan pembangunan menara blok yang mengesankan. Apakah Anda memperhatikan sesuatu saat membangun menara Anda? Balok-balok itu tidak secara ajaib mengubah bentuk, jumlah, atau ukurannya. Namun, tata letak blok berubah.
Ini adalah contoh isomer yang bagus! Isomer adalah senyawa yang rumus molekulnya sama tetapi struktur kimianya berbeda. Semakin besar molekul dan semakin bercabang, semakin besar jumlah isomer yang dapat dihasilkannya.
Berbagai jenis isomer
Isomer dapat dibagi menjadi dua kategori besar: isomer konstitusional dan stereoisomer.
isomer konstitusional
Isomer konstitusional adalah senyawa di mana atom terhubung atau terikat secara berbeda. Isomer ini juga dapat disebut sebagai isomer struktural. Mari kita lihat contoh kumpulan blok kita. Jika ada penghubung atau batang yang menghubungkan satu balok ke balok lainnya dan Anda baru saja mengubah penghubung tersebut, himpunan balok (a) akan menjadi isomer konstitusional dari kumpulan balok (b) dan sebaliknya. Ingat saja, struktur kimianya berubah, bukan formulanya.
stereoisomer
Stereoisomer adalah senyawa yang berbeda berdasarkan orientasinya dalam ruang. Saya tahu Anda mungkin berpikir, apa hubungannya ruang dengan kimia? Pikirkan seperti ini: Bayangkan Anda dapat mengambil struktur kimia dari selembar kertas dan mulai memutar atom dan ikatan, memutar molekul, memutarnya ke arah yang berbeda. Kemampuan ini mengacu pada geometri molekuler atau stereokimia suatu senyawa. Ini adalah orientasi atau susunan 3D atom dalam suatu senyawa. Ada dua jenis stereoisomer: enansiomer dan diastereomer. Coba bayangkan secara visual susunan spasial dari molekul-molekul ini.
enansiomer
Enansiomer adalah jenis stereoisomer di mana senyawanya merupakan bayangan cermin satu sama lain. Gambar cermin ini tidak boleh tumpang tindih. Cara yang bagus untuk memahami konsep gambar yang tidak dapat ditumpangkan adalah dengan melakukan latihan ini dengan tangan Anda:
Ambil tangan kanan Anda (telapak tangan ke bawah) dan letakkan di atas tangan kiri Anda. apa yang kamu perhatikan? Ibu jari kanan menghadap ke arah yang berbeda dari ibu jari kiri. Tangan kanan tidak boleh tumpang tindih dengan tangan kiri karena jari-jari tidak akan cocok satu sama lain. Kemampuan untuk menjadi non-superimposable ini mendefinisikan molekul kiral. Kiralitas adalah molekul yang memiliki bayangan cermin dan tidak dapat ditumpangkan.
diastereomer
Diastereomer adalah isomer yang bukan bayangan cermin satu sama lain dan tidak dapat tumpang tindih. Ini adalah kebalikan dari enansiomer. Ada dua jenis diastereomer: cis dan trans. Isomer Cis mengandung atom yang berorientasi pada sisi ikatan yang sama. Isomer trans memiliki atom yang berorientasi pada sisi berlawanan dari suatu ikatan. Mari kita lihat beberapa gambar untuk memahami konsep-konsep ini.
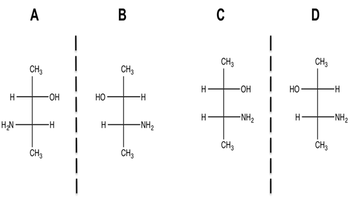
Di sini Anda dapat melihat gambar kerangka karbon isomer untuk 3-nitro-2-butanol:
|
|
Bayangkan garis putus-putus adalah cermin atau lipatan. Untuk molekul A dan B, dapatkah Anda melihat bahwa OH dan H berada pada posisi yang sama? NH 2 dan H juga berada di posisi yang sama. Ini memberi tahu Anda bahwa Anda sedang melihat gambar cermin. Sekarang jika Anda mencoba mengambil A dan meletakkannya di atas B, Anda akan melihat bahwa atom-atomnya tidak lagi cocok. Ini tidak dapat ditumpangkan. Oleh karena itu, A adalah enantiomer dari B dan sebaliknya.
Mari kita lihat diastereomer. Dalam C dan D, Anda akan melihat bahwa NH 2 dan H bukanlah bayangan cermin. C tidak bisa menjadi bayangan cermin dari D, dan jika Anda mencoba meletakkan C di atas D, atom H dan OH tidak cocok. Itu tidak bisa ditumpangkan. Jadi C adalah diastereomer dari D. Perhatikan juga bahwa H berada di sisi berlawanan dari D; ini disebut isomer trans. Di C, H berada di sisi yang sama; ini disebut isomer cis.
Selalu gambar kerangka karbon dan perhatikan susunan atom saat memutuskan apakah suatu molekul adalah enantiomer atau diastereoisomer.
Contoh isomer
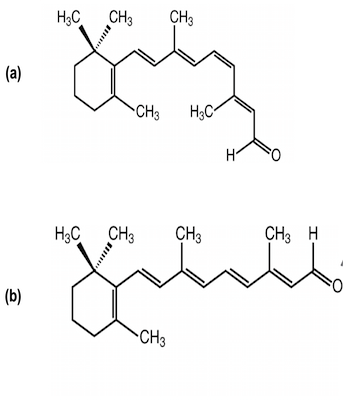
Konfigurasi atom dalam suatu senyawa sangat penting dalam biologi. Misalnya, kita memiliki protein di mata kita yang disebut rhodopsin. Protein ini memiliki isomer yang berbeda. Rhodopsin punya teman bernama retina. Terbuat dari vitamin A, retina juga memiliki isomer. Ketika retina berubah dari isomer cis menjadi trans, energi cahaya yang masuk ke mata kita diserap. Setelah retina mengambil energi cahaya yang diserap ini dan mengirimkannya ke rhodopsin, rhodopsin mengangkutnya melalui sistem penglihatan kita. Sebelum Anda menyadarinya, kami akan dapat melihat! Lihatlah dua isomer; perhatikan perubahan antara struktur isomer retina.
|
|
Ringkasan Pelajaran
Isomer adalah senyawa yang memiliki rumus molekul sama tetapi strukturnya berbeda. Ada dua jenis isomer: konstitusional dan stereoisomer. Isomer konstitusional berbeda dalam pengikatan dan konektivitas. Stereoisomer berbeda dalam orientasi 3D. Enantiomer dan diastereomer adalah dua subtipe stereoisomer. Enansiomer adalah isomer yang merupakan gambar cermin yang tidak dapat ditumpangkan. Diastereomer bukanlah bayangan cermin dan tidak dapat ditumpangkan. Diastereomer mencakup isomer cis dan isomer trans. Isomer banyak terdapat dalam biologi kehidupan. Isomerisasi Rhodopsin dan retina memainkan peran kunci dalam kemampuan kita untuk melihat.
hasil pembelajaran
Video ini akan membantu Anda:
- menentukan isomer
- Bedakan Antara Isomer Konstitusional dan Stereoisomer
- Bandingkan dan bedakan enansiomer dan diastereomer
- Membedakan antara isomer cis dan isomer trans
- Berikan contoh isomer