berbagai jenis apel
Saya selalu mendengar bahwa Anda tidak boleh membandingkan apel dengan jeruk, jadi saya akan memulai pelajaran ini dengan membandingkan apel dengan apel. Nanti, ini dapat membantu Anda mengingat bagaimana membandingkan dan membedakan isotop atom yang berbeda. Lebih khusus lagi, kami akan menjelaskan tiga jenis apel yang berbeda: Crabapple, Golden Delicious, dan Granny Smith, semuanya sangat berbeda tetapi semuanya apel.
Jadi apa yang membuat mereka apel? Mereka semua secara biologis disebut ‘malus domestica’. Mereka tumbuh di pohon. Mereka memiliki batang. Daftarnya terus berlanjut. Tapi apa yang membuat mereka berbeda? Pertama-tama, Crabapple sangat kecil, warnanya merah dan rasanya cukup asam. Untuk keperluan pelajaran ini, kami akan memberinya massa fiktif 1 amu, yang kami sebut ‘satuan massa apel’, sedangkan Golden Delicious berukuran sedang, berwarna kekuningan, rasanya manis, dan kami’ akan memberinya massa 2 sma. Terakhir, Granny Smith bertubuh besar, berwarna hijau, dan memiliki rasa yang pahit. Kami akan memberi apel ini massa 3 amu, sehingga beratnya tiga kali lipat dari Crabapple. Mereka semua serupa dalam arti bahwa mereka adalah apel, tetapi mereka memiliki banyak karakteristik yang berbeda. Jadi jika saya bertanya kepada Anda berapa massa sebuah apel, apa yang akan Anda katakan? 1 amu? dua? Atau 3 amu? Yah, itu semua tergantung pada jenis apel yang Anda maksud.
berbagai jenis atom
Sekarang, mari kita bandingkan atom-atomnya. Dalam pelajaran sebelumnya, Anda belajar tentang komposisi inti dan bagaimana mengandung proton dan neutron, keduanya merupakan kontributor utama massa atom (massa elektron tidak cukup signifikan untuk dilacak). Jumlah proton yang dimiliki suatu atom akan menentukan jenis unsurnya, dan semua atom dari unsur yang sama akan selalu memiliki jumlah proton yang sama. Yang menarik adalah jumlah neutron dalam nukleus. Kami akan menggunakan hidrogen sebagai contoh.
Hidrogen memiliki tiga isotop utama . Ingat bahwa isotop memiliki jumlah proton yang sama tetapi jumlah neutron yang berbeda. Isotop hidrogen yang paling umum hanya memiliki satu proton dan nol neutron. Jika proton dan neutron memiliki massa sekitar 1 amu (satuan massa atom), massa atom ini akan menjadi sekitar 1 amu (massa proton saja). Isotop hidrogen ini memiliki nama khusus, protium, dan merupakan lebih dari 99,98% dari semua atom hidrogen.
|
|
|
Protium adalah isotop utama yang ada dalam unsur hidrogen. |
Isotop paling umum berikutnya disebut deuterium. Intinya mengandung satu proton dan satu neutron, sehingga memiliki massa sekitar 2 sma. Jumlahnya kurang dari dua per seratus persen populasi atom hidrogen.
Isotop terakhir disebut tritium, dan seperti yang Anda duga, ia masih hanya memiliki satu proton, tetapi mengandung dua neutron dalam nukleusnya, sehingga massanya 3 amu. Ada sangat sedikit tritium dan sangat tidak stabil.
Jadi jika saya bertanya berapa massa atom hidrogen, Anda perlu tahu isotop mana yang saya bicarakan: protium, deuterium, atau tritium.
Ingatlah bahwa ketiga isotop ini semuanya secara kimiawi sama, seperti halnya tiga jenis apel kita yang hanya apel. Mereka semua masih hidrogen dan mereka semua akan bereaksi dengan cara yang sama. Misalnya, Anda mungkin tahu bahwa air (H2O) terdiri dari dua atom hidrogen dan satu atom oksigen. Apa yang mungkin tidak Anda ketahui adalah bahwa meskipun sebagian besar air yang Anda minum mengandung isotop protium hidrogen, ada beberapa molekul dalam gelas Anda yang mengandung isotop deuterium yang “lebih berat”. Apakah ini penting? Tidak terlalu. Tubuh kita mengandung sedikit air ‘berat’ dan kita baik-baik saja. Namun, kami tidak ingin membiasakan minum 100% air ‘berat’ setiap hari. Air ‘berat’ khusus ini digunakan di beberapa reaktor nuklir dan di beberapa laboratorium ilmiah.
|
|
|
Meskipun air mengandung dua isotop hidrogen, hanya ada sedikit deuterium. |
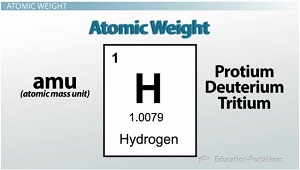
Berat atom
Sekarang, saya ingin mengalihkan perhatian Anda ke tabel periodik, lebih khusus lagi, blok hidrogen di pojok kiri atas. Lihat angka kecil di bawah simbol kimia itu? Itu disebut massa atom rata-rata (atau berat atom). Ingatlah bahwa satuan massa atom adalah amu (atau satuan massa atom). Jadi berapa massa isotop yang kita lihat? Protium, deuterium atau tritium? Jawabannya adalah semua orang.
Berat atom pada tabel periodik dihitung berdasarkan kelimpahan relatif dari setiap isotop unsur tersebut. Ini benar-benar rata-rata tertimbang dari semua isotop alami. Jadi, karena sebagian besar hidrogen memiliki massa 1 sma, berat atom pada tabel periodik akan sangat mendekati 1; namun, karena ada beberapa isotop hidrogen yang lebih berat, berat yang diwakili akan sedikit lebih tinggi dari 1 atau 1,0079 sma.
Contoh lain adalah litium. Ada dua isotop utama litium: litium-6, yang memiliki tiga proton dan tiga neutron, dan litium-7, yang memiliki tiga proton dan empat neutron. Menurut tabel periodik, berat atom adalah 6,941 sma. Berdasarkan ini, isotop mana yang menurut Anda paling umum? Litium-6 atau litium-7? Karena angka 6.941 jauh lebih dekat dengan 7, kemungkinan lebih banyak litium-7 yang ada di alam. Perhatikan bahwa, seperti apel dan atom hidrogen, kedua isotop litium akan memiliki perilaku yang serupa. Satu-satunya perbedaan mereka adalah massa mereka.
|
|
|
Berat atom suatu unsur termasuk berat semua isotop. |
Karena sebagian besar perhitungan kita akan mengacu pada populasi umum atom dan bukan pada isotop tertentu, kita akan menggunakan nilai berat atom ini di sebagian besar pelajaran dalam kursus ini. Oleh karena itu, penting untuk mengetahui cara menghitungnya dan apa artinya sebenarnya. Selain itu, perlu diingat bahwa setiap tabel periodik dapat terlihat berbeda dari yang berikutnya, jadi pastikan Anda memahaminya sebelum mulai menghitung.
Ringkasan Pelajaran
Isotop hanyalah variasi dari unsur yang sama; mereka memiliki jumlah proton yang sama dan semuanya akan bereaksi dengan cara yang sama. Satu-satunya perbedaan adalah mereka memiliki jumlah neutron yang berbeda, yang akan membuat massa mereka berbeda. Kelimpahan setiap jenis isotop diperhitungkan saat menghitung massa atom rata-rata, atau berat atom, yang ditemukan di tabel periodik.
Hasil belajar
Setelah menonton pelajaran ini, Anda akan dapat mengenali bagaimana isotop adalah variasi dari unsur yang sama dan bagaimana isotop diperhitungkan saat menghitung massa atom.