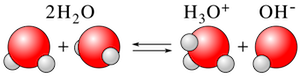Asam dan basa
Apa kesamaan isi perut Anda, baterai mobil Anda, dan segelas jus jeruk? Cairan yang tampaknya berbeda ini semuanya adalah contoh asam. Di ujung spektrum kami memiliki basa, yang mencakup contoh mulai dari pemutih rumah tangga hingga soda kue yang Anda gunakan untuk membuat kue. Kemungkinan besar contoh-contoh ini dan bahkan konsep asam dan basa sudah tidak asing lagi bagi Anda. Namun dalam sains, apa yang membuat sesuatu menjadi asam atau basa?
Ada beberapa definisi, tetapi di sini kita akan tetap menggunakan definisi Bronsted Lowry. Definisi ini mengatakan bahwa asam adalah molekul yang dapat menyumbangkan ion hidrogen, juga disebut proton. Sedangkan basa adalah molekul yang dapat menerima ion hidrogen. Asam klorida di perut Anda menyumbangkan proton ke molekul lain, yang membantu memecah strukturnya dan mengubahnya menjadi asam. Natrium hidroksida dalam pemutih dapat menerima ion hidrogen, mengubahnya menjadi basa.
Air
Air adalah molekul khusus dan memiliki banyak sifat unik yang menjadikannya penting bagi semua kehidupan di Bumi. Faktanya, ketika para ilmuwan mencari kehidupan di planet lain, mereka mencari tanda-tanda adanya air terlebih dahulu! Air terdiri dari dua atom hidrogen yang terikat pada satu atom oksigen. Mereka membentuk ikatan ini dengan berbagi elektron.
Namun, oksigen sangat tidak baik untuk berbagi. Oksigen sangat elektronegatif , artinya ia menyukai elektron. Dengan demikian, ia menarik elektron dalam ikatan lebih dekat ke dirinya sendiri, menyebabkan oksigen memperoleh muatan parsial negatif dan atom hidrogen memperoleh muatan parsial positif. Hal ini memungkinkan air untuk membentuk ikatan antara molekul yang berbeda berdasarkan muatan, yang disebut ikatan hidrogen. Ini memberi air banyak sifat uniknya yang memungkinkannya mendukung kehidupan.
Air juga memiliki sifat penting bertindak sebagai asam atau basa tergantung pada kondisinya. Air melewati autoionization , di mana satu molekul air dapat menyumbangkan atom hidrogen yang lain. Ini membentuk ion hidroksida (OH-) dan ion hidronium (H3O+). Dalam contoh ini, air bertindak sebagai asam, menyumbangkan ion hidrogen, dan basa, menerima ion hidrogen.
|
|
|
Selama autoionisasi, air bertindak sebagai asam dan basa. |
air sebagai asam
Ketika air bertindak sebagai asam, ia menyumbangkan ion hidrogen ke molekul lain dan menjadi molekul hidroksida (OH-). Mari kita lihat contohnya. Misalkan Anda ingin mengencerkan produk pembersih yang sebagian besar terbuat dari amonia, NH3, dengan air. Amonia adalah basa yang menerima atom hidrogen menjadi amonium atau NH4+. Ketika amonia dicampur dengan air, amonia adalah basa yang lebih kuat, sehingga air menyumbangkan ion hidrogen yang membentuk ion amonium dan hidroksida.
Air sebagai Dasar
Namun, ketika air bertindak sebagai basa, terjadi sebaliknya. Air menerima ion hidrogen untuk menjadi molekul hidronium. Katakanlah Anda mencoba berhenti menggunakan bahan kimia keras seperti amonia untuk membersihkan rumah Anda. Anda telah membaca bahwa cuka sari apel juga bisa bekerja. Anda memutuskan untuk mengencerkan cuka ke dalam air untuk membuat larutan pembersih untuk dapur Anda. Cuka adalah asam lemah yang disebut asam asetat dengan rumus molekul CH3COOH, tetapi masih merupakan asam yang lebih kuat dibandingkan dengan air. Ketika dicampur dengan air, asam asetat menyumbangkan ion hidrogen ke air. Ini menghasilkan ion hidronium dari air.
Air juga dapat bertindak sebagai basa dengan asam yang lebih kuat. Perut kita penuh dengan asam klorida (HCl). Ketika air dicampur dengan asam klorida, air bertindak sebagai basa dan menerima ion hidrogen dari asam klorida. Ini menciptakan ion hidronium dan ion klorin.
Ringkasan Pelajaran
Asam adalah molekul yang dapat menyumbangkan ion hidrogen dan basa adalah molekul yang dapat menerima ion hidrogen, seperti yang didefinisikan oleh Bronsted Lowry. Air dapat bertindak sebagai asam dan basa dalam larutan dan terionisasi sendiri di mana ia dapat menjadi asam dan basa itu sendiri. Ketika dicampur dengan asam, air menerima ion hidrogen dan bertindak sebagai basa. Namun, ketika air dicampur dengan basa, ia menyumbangkan ion hidrogen dan bertindak seperti asam.